|
|
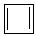
Приведите электронные конфигурации атома углерода, кислорода и азота в основном и возбужденном состояниях.ПРАКТИЧЕСКИЕ ЗАНЯТИЯ Раздел I. Теоретические основы органической химии Практическое занятие «Номенклатура ИЮПАК органических соединений. Классификация органических соединений». Воросы и упражнения: 1. Укажите, какое число соединений обозначено приведенными ниже структурными формулами: C2H5 CH3 | | СH3-C-CH3 CH-CH3 3. CH3-CH2-CH2-CH3 | | 1. CH3 2. CH3
CH3 CH3 | | 4. CH3-C-CH2 –CH3 5. CH2-CH2 –CH3 6. HC(CH3)3 │ СН3 7.
10. 2. Среди представленных соединений укажите моно-, поли - и гетерофункциональные соединения ациклического и циклического строения: а) НООС-СН2-СН2-СООН в) НОСН2-СН2ОН б) СН2=СН-СН=О г) Н3С-СНОН-СН2-СООН д) е)
Укажите, к каким классам относятся данные соединения. 3. Укажите основные правила номенклатуры ИЮПАК. Назовите соединения по заместительной номенклатуре ИЮПАК: а) CH3-CH2-CH=O б) CH3-CO-CH2-CH2OH
4. Напишите структурные формулы соединений: а) 3-бутеновая кислота; б) 2-гидроксипентаналь; в) 1,5-гексадиен-3-ин; г) 2,3- дикарбоксигептандиовая кислота. Практическое занятие «Химическая связь в органических соединениях. Взаимное влияние атомов в органических соединениях». Воросы и упражнения: Дайте характеристику основным типам связи в молекулах органических соединений. Примеры. Ковалентная связь, ее разновидности. Примеры.
Приведите электронные конфигурации атома углерода, кислорода и азота в основном и возбужденном состояниях.
3. Типы гибридизации атомных орбиталей элементов 2 периода: sр3, sр2, sр – гибридизация (на примере атома углерода). 4. Укажите типы гибридизации атомов углерода, азота и кислорода в соединениях: а) СH3CH2OH; б) CH2=C=CH-CH3; в) CH3NH2; г) CH≡C-CH=O; д) CH3 –С≡N; е) Укажите число гибридизованных и негибридизованных атомных орбиталей, количество σ- и π- связей, величину валентного угла для каждого атома углерода, кислорода, азота. Дайте характеристику пространственного строения соединений.
5. Ковалентные σ- и π- связи в органических соединениях. Учитывая форму и пространственную направленность атомных орбиталей атомов, графически изобразите схему образования локализованных σ- и π- связей в молекуле бутин-3-аля (атомно-орбитальная модель). Укажите типы перекрывания атомных орбиталей.
6. Дайте характеристику основным типам межмолекулярного взаимодействия. Что такое водородная связь? Рассмотрите условия образования и виды водородной связи.
7. В каких из указанных ниже соединений следует ожидать образования водородных связей? Укажите их тип, представьте схему их образования:
Сравните температуры кипения соединений в приведенных парах: а) и в); б) и в).
8. Индуктивные электронные эффекты. ( +I, - I). Рассмотрите распределение электронной плотности в бутаноле-1. 9. Мезомерные электронные эффекты (+М, -М, М).Укажите графически распределение электронной плотности в бутанале, бутене – 1, бутен-2-але и бутен-1-оле-2. Укажите виды сопряжения в этих соединениях. Напишите мезоформулы соединений.
10. Укажите, в каких случаях в соединениях группа -NH2 проявляет электронодонорные, а в каких - электроноакцепторные свойства: a) CH3-CH2-NH2, CH3-CH=CH-NH2, CH2=CH-CH2-NH2? Укажите графически электронные эффекты в данных соединениях. Практическое занятие « Изомерия». Воросы и упражнения: 1. Структурная изомерия, основные виды. Для каждого вида структурной изомерии приведите по 2-3 примера структурных изомеров состава С5Н10О, назовите их по заместительной номенклатуре ИЮПАК. Укажите, к каким классам соединений относятся данные изомеры. 2. Геометрическая изомерия (цис, транс, Z-, Е). Какие из указанных соединений образуют геометрические изомеры: 1,1-дихлорциклопропан; 2-хлорбутен-2; 1,2 – диэтилциклогексан; 2,3-диметилбутен-2; 3-бромпентен-2? Представьте геометрические изомеры в виде проекций. Назовите изомеры, сравните их некоторые свойства (температура кипения, плавления, плотность, полярность и стабильность молекул).
3. Оптическая изомерия.Понятие о хиральности. Соединения с одним и двумя асимметрическими атомами углерода: энантиомеры, диастереомеры, мезоформы. Способы изображения оптических изомеров. Номенклатура оптических изомеров. Укажите соединения, молекулы которых хиральны: 2-пропанол; пентанол-2; бутандиол-2,3; пентандиол-2,3. В молекулах укажите число асимметрических атомов углерода. Изобразите с помощью проекционных формул Фишера оптические изомеры. Укажите энантиомеры, диастереомеры, мезоформы. Определите конфигурации асимметрических центров оптических изомеров (R, S- конфигурации).
Раздел II. Углеводороды. Практическое занятие «Обобщение по разделу II «Углеводороды». Воросы и упражнения: 1. Что такое гомологический ряд и гомологическая разность?По какому признаку объединяют вещества в гомологические ряды? Среди представленных ниже соединений укажите гомологи и изомеры: а) С4Н9-СН=СН2; б) (СН3)3С-СН2-СН3; в) СН4; г) СН3-(СН2)4-СН3; д) С2Н5-С≡С-С2 Н5; е) СН2=С(СН3)С(СН3)=СН2; к)
2. Назовите следующие соединения по двум номенклатурам - ИЮПАК и рациональной: (СН3)2СН – С≡С – СН3 ; СН2 = С(С2 Н5)2 ; (С2Н5)2С=СН-СН3.
3. На примере пропина рассмотрите схемы образования σ- и π -связей,укажите все электронные эффекты в данном соединении.
4. Напишите структурные формулы ароматических соединений: о-диэтилбензола; п-толуолсульфокислоты; м-нитротолуола; о-ксилола.
5. Определите, какие из перечисленных соединений обладают ароматичностью:
6. Осуществите превращения и назовите промежуточные и конечные продукты превращений:
а) при сплавлении соли СН3СН2СН2СН2СООNа с натронной известью и последовательном действии на полученное соединение следующих реагентов: хлорида алюминия (t); 1 моль брома (t); Nа(t)
КОН Н2О Аl2 О3 НОСl б) 1-бром-3-метилбутан → А → В → С → Д. спирт H2 SО4 300оС
в) метан - нагревание до t=14000С и последовательное действие на полученное соединение следующих реагентов: 1моль[Сu(NH3)2]Cl; СН3Cl(t); (р-р) НСI; Н2О (в присутствии H2 SО4);
г) Na 1Н2 Сl2 Н2 О Бромэтен → А → В → С → Д . t ˃00С
д) в результате последовательного действия на бензол следующих реагентов: Cl2 (в присутствии FeCl3); С2Н5Cl (в присутствии металлического натрия); НNО3 (в присутствии серной кислоты); уксусного ангидрида (в присутствии FeCl3); Вr2 (при нагревании). 
Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2024 stydopedia.ru Все материалы защищены законодательством РФ.
|
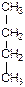 8.
8.  9.
9. 
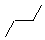 11.
11.  12. (СН3)3С(С2Н5).
12. (СН3)3С(С2Н5).






 ; ж)
; ж)  .
.
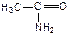

 ж)
ж)