|
|
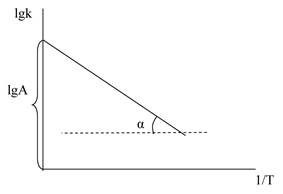
Методы расчета энергии активации.Расчет производится по уравнению Аррениуса: k = Ae -E/RT 1. Графический метод. Логарифмируем уравнение Аррениуса: lnk = lnA - E/RT или lgk = lgA - E/(2,303·RT), если R=1,987 кал К-1·моль-1, то lgk = lgA - E/(2,303·1,987 T) = lgA - E/4,575T. Строим график (рис. 5.5.):
Рис. 5.5. Расчет энергии активации.
tgα = -E /4,575, откуда E = -4,575·tgα [кал/моль]. 2. Аналитический метод. Е = (4,575lg·k2/k1)/(1/T1 - 1/T2) = = 4,575´Т1´Т2´lg·(k2/k1) /(Т2-Т1).
Сложение реакции. Сложенными называются реакции, состоящие из нескольких простых реакций. Простыми называются реакции, протекающие в одну стадию. В основе кинетики сложных реакций лежит принцип независимого протекания отдельных реакций: если в системе одновременно протекает несколько реакций, то каждая из них протекает независимо, подчиняясь закону действующих масс. Общее изменение системы равно сумме всех этих независимых переменных. К сложным реакциям относятся: обратимые, параллельные, последовательные, сопряженные. Обратимыми называются реакции, которые протекают одновременно в двух противоположных направлениях. Простейший тип - реакции первого порядка. Параллельные реакции - реакции, в которых исходные вещества одновременно реагируют в нескольких направлениях. Последовательные реакции - если какой либо продукт, образующийся в одной из реакций, расходуется в другой. Сопряженные реакции - это сложные реакции, в которых одна реакция идет только в присутствии другой: А + В → P + Q (1), A + C → R + S (2) Для сопряженных реакций не выполняется принцип независимости отдельных реакций. Это пример химической индукции, когда одна реакция индуцирует вторую. Первая реакция - первичная, вторая - вторичная. Вещество, которое принимает участие в обеих реакциях, называется актором (А). Вещество, которое реагирует с актором в первичной реакции, называется индуктором (В). Вещество, которое реагирует с актором во вторичной реакции, называется акцептором (С). В изолированных аппаратах реакция (1) идет с достаточной скоростью, а реакция (2) - медленно. Если эти реакции вести в одном аппарате, то они обе протекают с достаточной скоростью, т.е. вторая реакция индуцируется первой. Механизм этих реакций сводится к образованию промежуточных соединений, которые ускоряют вторую реакцию. Например, перекись водорода окисляет двухвалентное железо в трехвалентное. Эта реакция протекает легко, но окисление бензола перекисью водорода идет медленно. Можно сказать, что бензол перекисью водорода практически не окисляется. Однако, если окислить ионы двухвалентного железа перекисью водорода в присутствии бензола, то оказывается, что бензол окисляется перекисью водорода. (1) Fe2+ + H2O2 = Fe3+ + ÓH + OH- (2) ÓH + C6H6 = Ć6H5 + H2O Ć6H5 + OH- = C6H5OH H2O2 - актор; ионы Fe2+ - индуктор; бензол - акцептор. Явление химической индукции было детально изучено Н.А. Шиловым (1905 г). В зависимости от концентрации индуктора во времени, Шилов Н.А. разделил сопряженные реакции на 3 типа: 1) собственно-сопряженные - концентрация индуктора во времени убывает; 2) каталитические реакции - концентрация индуктора не меняется; 3) автокаталитические или самоускоряющиеся реакции - концентрация индуктора возрастает. Автокаталитические - реакции, в которых один из продуктов реакции является катализатором. Механизм сопряженных реакций может быть представлен так: актор + индуктор → М (промежуточное соединение); М + индуктор → продукт 1-ой реакции: М + акцептор → продукт 2-ой реакции. Цепные реакции.
В природе существует многочисленные реакции, которые не подчиняются уравнению Аррениуса, закону действующих масс. Скорости протекания таких реакций нельзя объяснить ни одной теорией кинетики, уравнениями формальной кинетики. Это и есть цепные реакции. Цепными реакциями называется реакции, протекающие с участием химически активных частиц (свободные атомы и радикалы) и состоящие из большого количества повторяющихся стадий. К цепным реакциям относятся реакции горения, медленного окисления, радиоактивного распада, передачи нервного импульса, ядерные реакции и т.д. К характерным особенностям цепных реакций относятся: 1) скорость реакции не совпадает со скоростью, вычисленной по теории активных соударений, т.е. υнаблюдаемая >> υ расчета; 2) исключительная чувствительность к примесям положительных и отрицательных катализаторов, которые ускоряют или замедляют реакцию; 3) зависимость скорости реакции от размеров, формы, материалов сосуда. В сосуде большего объема скорость реакции больше. Скорость реакции замедляется, если в свободное пространство поместить осколки кварца, стекла, фарфора и т.п. 4) Наличие нижнего и верхнего пределов воспламенения или взрыва для реакций окисления газов, ниже и выше которых реакции идут медленно или вообще не идут. Особенности протекания этих реакций объясняется цепным механизмом реакции, в разработку которого существенный вклад был внесен академиком Н.Н. Семеновым (рис. 5.6). Активная частица “А”, образовавшаяся путем столкновения или любым другим путем, может дезактивироваться, но может дать промежуточное вещество “Z”, которое в свою очередь может разложиться без образования продуктов или дать продукты реакции и новую активную частицу. При этом, активация одной молекулы исходных веществ приводит к образованию большого количества молекул продуктов реакции.
Рис. 5.6. Схема цепной реакции.
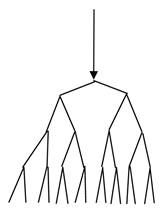
Основные положения теории цепных реакций: 1) в реакции участвуют атомы или свободные радикалы (частицы, имеющие не спаренный электрон). Атом или свободный радикал обладают исключительной активностью по отношению к валентно-насыщенной молекуле; 2) при взаимодействии валентно-насыщенной молекулы с атомом или свободным радикалом “свободная валентность” не исчезает, а дает начало новой активной частице (принцип неучтожимости свободной валентности). Под “свободной валентностью” надо понимать частицы, имеющие неспаренный электрон (атом или свободный радикал). Основные стадии цепной реакции: 1) зарождение цепи - элементарная стадия цепной реакции, приводящая к образованию свободной валентности из валентно-насыщенной молекулы; 2) продолжение или развитие цепи - элементарная стадия, идущая с сохранением свободной валентности и приводящая к расходованию исходных веществ и образованию продуктов реакции; 3) обрыв цепи - элементарная стадия, приводящая к исчезновению свободной валентности. Пример цепной реакции - синтез HCl. H2 + Cl2 = 2HCl 1. Зарождение цепи (возбуждение, инициирование): Cl2 + hν = 2Cl˙ (Eдиссоц Cl2 = 57 кал/моль), H2 + hν = 2H˙ (Едиссоц H2 = 103,3 кал/моль). Так как энергия связи молекулы хлора ниже, то зарождение цепи идет за счет диссоциации молекул Cl2. 2. Продолжение или развитие цепи: Cl˙ + H2 = HCl + H˙, H˙+Cl2 = HCl + Cl˙,т.е. свободная валентность не исчезает. 3. Обрыв цепи: H˙+ H˙+ стенки = H2 Сl˙+Cl˙ + стенки = Cl2 H˙+Cl˙ + стенки = HCl Возможен обрыв цепи за счет рекомбинации свободных радикалов (гомогенный процесс) и гетерогенный процесс - обрыв цепи за счет стенок сосуда. В рассмотренном примере цепной реакции каждая активная частица дает начало одной цепи - это стационарная неразветвленная цепная реакция. Разветвленные цепные реакции – это реакции, в которых стадия развития цепи протекает с увеличением числа “свободных валентностей”. Схема ее выглядит следующим образом:
Рис. 7. Схема разветвленной реакции.
Пример разветвленной реакции - синтез воды при высокой температуре. 2H2 + O2 = 2H2O 1. Зарождение цепи: H2 + O2 = 2OH˙, OH˙+ H2 = H2O + H˙ 2. Развитие цепи: H˙+ O2 = OH˙ + Ö (бирадикал) Ö + H2 = OH˙ + H˙, H˙+ O2 + Н2 = 2OH˙ + H˙ -стадия развития цепи. Из одной активной частицы получается несколько, каждая из которых дает начало своей цепи. 3. Обрыв цепи: 2H˙ = H2 2ÓH = H2O2

Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2024 stydopedia.ru Все материалы защищены законодательством РФ.
|