|
|
В углеводородах главную роль играет пространственная ориентация атомных орбиталей углерода. Сферическая 1s-АО атома водорода лишена определенной направленности.Алканы – алифатические (ациклические) предельные углеводороды, в которых атомы углерода связаны между собой простыми (одинарными) связями в неразветвленные или разветвленные цепи. Алканы – название предельных углеводородов по международной номенклатуре. Парафины– исторически сложившееся название, отражающее свойства этих соединений (от лат. parrum affinis – имеющий мало сродства, малоактивный). Предельными, или насыщенными, эти углеводороды называют в связи с полным насыщением углеродной цепи атомами водорода. Простейшие представители алканов:
При сравнении этих соединений видно, что они отличаются друг от друга на группу –СН2– (метилен). Добавляя к пропану еще одну группу –СН2–, получим бутан С4Н10, затем алканы С5Н12, С6Н14 и т.д. Можно вывести общую формулу алканов. Число атомов углерода в ряду алканов примем за n, тогда число атомов водорода составит величину 2n+2. Следовательно, состав алканов соответствует общей формуле CnH2n+2. Алканы - углеводороды, состав которых выражается общей формулой CnH2n+2, где n – число атомов углерода. Зависимость количества атомов углерода от относительной молекулярной массы. Мr (CnH2n+2) = Аr (С) + Аr (Н) = 12n + 2n + 2 = 14n + 2. Mr = 14n + 2
Гомологический ряд алканов.
Алканы, имея общую формулу СnH2n+2, представляют собой ряд родственных соединений с однотипной структурой, в котором каждый последующий член отличается от предыдущего на постоянную группу атомов (-CH2-). Такая последовательность соединений называется гомологическим рядом (от греч. homolog – сходный). Отдельные члены этого ряда – гомологами. Группа атомов, на которую различаются соседние гомологи, – гомологической разностью. Гомологический ряд алканов легко составить, прибавляя каждый раз к предыдущей цепочке новый атом углерода и дополняя его оставшиеся валентности до 4-х атомами водорода. Другой вариант – добавление в цепь группы ––– (СН2) – CH4 или Н-СН2-Н – первый член гомологического ряда – метан (содержит 1 атом C); CH3-CH3 или Н-СН2-СН2-Н – 2-й гомолог – этан (2 атома С); CH3-CH2-CH3 или Н-СН2-СН2-СН2 -Н – 3-й гомолог – пропан (3 атома С); CH3-CH2-CH2-CH3 или Н-СН2-СН2-СН2-СН2-Н – бутан (4 атома С). Суффикс -ан является характерным для названия всех алканов. Начиная с пятого гомолога, название алкана образуется из греческого числительного, указывающего число атомов углерода в молекуле, и суффикса -ан: пентан С5Н12, гексан С6Н14, гептан С7Н16, октан С8Н18, нонан С9Н20, декан С10Н22 и т.д. Гомологи отличаются молекулярной массой, следовательно, физическими характеристиками. С увеличением числа углеродных атомов в молекуле алкана (с ростом молекулярной массы) в гомологическом ряду наблюдается закономерное изменение физических свойств гомологов (переход количества в качество): повышаются температуры кипения и плавления, увеличивается плотность. Алканы от СН4 до С4Н10– газы, от С5Н12 до С17Н36 – жидкости, далее – твердые вещества. Имея одинаковый качественный состав и однотипные химические связи, гомологи обладают сходными химическими свойствами. Поэтому, зная химические свойства одного из членов гомологического ряда, можно предсказать химическое поведение и других членов этого ряда. Гомологами называются вещества сходные по строению и химическим свойствам и отличающиеся друг от друга на – СН2 – группу (называемую гомологической разностью) и имеющими разные физические свойства. Для получения гомологов используются общие методы синтеза. Строение алканов Химическое строение (порядок соединения атомов в молекулах) простейших алканов – метана, этана и пропана – показывают их структурные формулы.
Из этих формул видно, что в алканах имеются два типа химических связей: С–С и С–Н.Связь С–С является ковалентной неполярной. Связь С–Н - ковалентная слабополярная, т.к. углерод и водород имеют близкие значения электроотрицательности. Электронные и структурные формулы отражают химическое строение, но не дают представления о пространственном строении молекул, которое существенно влияет на свойства вещества. Пространственное строение, т.е. взаимное расположение атомов молекулы в пространстве, зависит от направленности атомных орбиталей (АО) этих атомов. В углеводородах главную роль играет пространственная ориентация атомных орбиталей углерода. Сферическая 1s-АО атома водорода лишена определенной направленности. Пространственное расположение АО углерода в свою очередь зависит от типа его гибридизации. Насыщенный атом углерода в алканах связан с четырьмя другими атомами. Следовательно, его состояние соответствует sp3-гибридизации. В этом случае каждая из четырех sp3-гибридных АО углерода участвует в осевом (s-) перекрывании с s-АО водорода или с sp3-АО другого атома углерода, образуя s-связи С-Н или С-С.
Четыре s-связи углерода направлены в пространстве под тетраэдрическим углом 109о28'. Поэтому молекула простейшего представителя алканов – метана СН4 – имеет форму тетраэдра, в центре которого находится атом углерода, а в вершинах – атомы водорода.
Валентный угол Н-С-Н равен 109о28’. Пространственное строение метана можно показать с помощью объемных (масштабных) и шаростержневых моделей. Для записи удобно использовать пространственную (стереохимическую) формулу.
В молекуле следующего гомолога – этана С2Н6 – два тетраэдрических sp3- атома углерода образуют более сложную пространственную конструкцию.
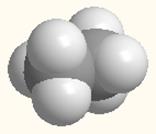
Шаростержневая и масштабная модели этана Для молекул алканов, содержащих свыше 2-х атомов углерода, характерны изогнутые формы. Это можно показать на примере н-бутана, или Н-пентана: показать с помощью объемных (масштабных) и шаростержневых моделей.
Шаростержневая и масштабная модели бутана
Номенклатура Номенклатура органических соединений – система правил, позволяющих дать однозначное название каждому индивидуальному веществу. 
Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2024 stydopedia.ru Все материалы защищены законодательством РФ.
|